
А.И. Яременко, к.м.н., доцент кафедры хирургической стоматологии и челюстно-лицевой хирургии СПбГМУ им. акад.И.П. Павлова
С.Ю. Виноградов, врач, клинический ординатор кафедры хирургической стоматологии и челюстно-лицевой хирургии СПбГМУ им. акад. И.П. Павлова
.
Некоторые аспекты терапии сопровождения при использовании антибактериальных препаратов в клинической стоматологии
  Инфекционные процессы встречаются в практике врача любой специальности. Для устранения инфекции необходима этиотропная терапия, направленная на ослабление или прекращение жизнедеятельности возбудителя. Для этих целей используются противомикробные химиотерапевтические средства. Инфекционные процессы встречаются в практике врача любой специальности. Для устранения инфекции необходима этиотропная терапия, направленная на ослабление или прекращение жизнедеятельности возбудителя. Для этих целей используются противомикробные химиотерапевтические средства.
Рациональная антибиотикотерапия - это искусство врача, основанное на знании и комплексном учете всех ее многочисленных аспектов (микробиологических, фармакокинетических, клинических, фармакоэкомических); она должна включать назначение собственно антибактериального препарата, "терапии сопровождения" и реабилитационного комплекса мероприятий после окончания лечения.
В настоящее время применение противомикробных средств занимает основное место в комплексной терапии для профилактики и лечения инфекционно-воспалительных заболеваний челюстно-лицевой области (Колесов А.П. и др., 1989; Жижина Н.А. и др., 1996; Хаитов Р.М., Пинегин Б.В., 1996; Шаргородский А.Г. и др., 1996; Бернадский Ю.И., 2000; Соловьев М.М., Большаков О.П., 2001; Тимофеев А.А., 2002, и др.). Применение противомикробных препаратов оказывает значительные воздействия на различные звенья гомеостаза, вызывая аллергические реакции, дисбиотические и иммуносупрессивные состояния, а также токсические влияния на внутренние органы (ото-, нефро-, гепато-, нейротоксичность и т.д.), что сопровождается нарушением выделения и детоксикации продуктов метаболизма. Для предотвращения развития побочных эффектов и осложнений необходимо параллельно с антибактериальной терапией назначать комплекс препаратов для "терапии сопровождения".
Достаточно остро перед клиницистами стоит проблема коррекции дисбиотических состояний, так как широкое использовании антимикробных химиопрепаратов, тотально воздействующих на патогенную и нормальную микрофлору, приводит к нарушению естественного равновесия в микробных ассоциациях (Шендеров Б.А., 1998; Петров Л.Н., 2002, Суворов А.Н., 2004). Тем не менее микробиоценозы обладают способностью к саморегуляции, но имеют некоторые пределы устойчивости, за которыми наступают изменения качественного и количественного состава нормальной микрофлоры, так называемые дисбактериозы. Этот процесс начинается с незначительных нарушений микрофлоры и клинически проявляется в виде дисбиотического сдвига, дисбактериоза 1-й - 4-й степеней (Ефимович О.И., Рабинович И.М., Рабинович О.Ф., Разживина Н.В., Дмитриева Н.А., 2001).
Говоря о микроэкологических нарушениях и их роли в возникновении заболеваний, как правило, ограничиваются рассмотрением патологических процессов в гастроинтестинальном аппарате, заблуждаясь, что изменения внутренней микробной экологии возможны не только в кишечнике. Но согласно положениям медицинской микробной экологии микробиоценозы слизистых оболочек образуют единый экстракорпоральный орган человека, выполняющий совокупность физиологических функций: трофической, иммунорегулирующей, антагонистической по отношению к патогенным микроорганизмам и др. Следовательно, важной особенностью дисбиоза является его системный характер (Суворов А.Н., 2004). Таким образом, поддержание состава нормальной микрофлоры является своего рода биологическим барьером, безопасной нишей для макроорганизма. При нарушении состава резидентной (постоянной) микрофлоры открываются сайты адгезии на поверхности слизистой оболочки, раневой поверхности и т.д. и активизируются патогенные и условно-патогенные микроорганизмы, которые колонизируют биотоп, размножаются в нем и вызывают заболевание (рис. 1).
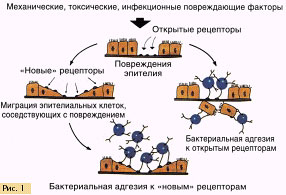
В клинической практике для коррекции нарушений внутренней микробной экологии используются различные препараты:
1. Пробиотики - это препараты, содержащие живые, активные микроорганизмы и их метаболиты, которые сохраняют или восстанавливают состав нормальной микрофлоры. Пробиотики могут содержать как монокультуру - один штамм микроорганизма (Лактобактерин, Бифидумбактерин, Бифилин, Ацилакт, Нормофлорин и др.), так и представлять механическую композицию разных видов микроорганизмов (Линекс, Бификол, Бифилонг и др.). Комбинированные препараты, содержащие виды микроорганизмов, образующих симбиоз, именуются симбиотиками (Витафлор). Препараты последней группы более эффективны, так как симбиоз бактерий усиливает их полезные свойства.
2. Пребиотики - препараты, не содержащие живых микроорганизмов и селективно стимулирующие рост и активность симбионтной микрофлоры (Лактулоза, Хилак-Форте и др.).
3. Синбиотики - комплексные препараты про- и пребиотиков (Бифиформ, Ламинолакт и др.).
По нашему мнению, применение пробиотических препаратов этиопатогенетически обосновано, так как содержащиеся в их составе жизнеспособные микроорганизмы, помимо восстановительной функции микробиоценозов, сами обладают антагонизмом по отношению к патогенной и условно-патогенной микрофлоре и участвуют в регуляции каскада иммунологических реакций (Шендеров Б.А., 1998; Петров Л.Н., 2002). Механизм лекарственного действия пробиотических препаратов можно представить, опираясь на данные по ауторегуляции в бактериальных популяциях. При попадании в организм штамм пробиотического микроорганизма выделяет в окружающую среду низко- и высокомолекулярные метаболиты. Низкомолекулярные метаболиты влияют на состав микробиоцинозов, восстанавливая его, в то время как высокомолекулярные метаболиты ответственны за проявления антагонистической активности по отношению к патогенным и условно-патогенным микроорганизмам. Кроме того, метаболиты разной химической природы и различного молекулярного веса обладают иммуномодулирующим действием (Nicole M. de Roos and Martijin B. Katan, 2000). Поэтому нельзя не согласиться с предложением академика Воробьева А.В. называть пробиотики иммунобиотиками.
Вместе с тем, как показывает клиническая практика, эффективность пробиотической терапии зависит от грамотного применения препарата определенного типа, лекарственной формы, способа и схем его применения.
 На наш взгляд, одним из перспективных препаратов для коррекции микроэкологических нарушений и восстановления иммунологической резистентности является пробиотик нового поколения симбиотического действия - Витафлор(r), разработанный в ГосНИИ ОЧБ, Санкт-Петербург (рис. 2). Наш выбор основывался на доказанной безвредности применения препарата, высокой метаболитической активности штаммовой культуры, уровне и спектре антагонизма и устойчивости к антибиотикам, выраженных адгезивных свойствах препарата, что определяет длительность действия. Отличительной особенностью препарата является наличие симбиотической биокультуры Lactobacillus аcidophilus (штаммы Д № 75 и Д № 76) (рис. 3). В отличие от моноштаммов, биокультура препарата характеризуется расширенным спектром и высоким уровнем антагонистической  активности в отношении клинических изолятов Гр(-) и Гр(+) бактерий и дрожжевых грибов рода Candida, выраженными адгезивными свойствами, высоким содержанием жизнеспособных клеток (не менее 5Ч108 КОЕ в одной дозе) (рис. 4). Штаммы биокультуры образуют симбиоз, что повышает жизнеспособность бактериальной основы, которая непосредственно коррелирует с терапевтической активностью препарата.
В качестве "терапии сопровождения" мы использовали сублингвальную форму препарата Витафлор(r) (по 1 таблетке 3 раза в день в период лечения и в течение 7 дней по окончании курса антибактериальной терапии), а также жидкую форму (1 флакон лиофильно-высушенной культуры растворяли в 100 мл воды и производили полоскания полости рта с последующим проглатыванием раствора 3 - 4 раза в день по 2 столовые ложки в течение курса антибактериальной терапии).
Для оценки эффективности применения препарата Витафлор(r) в стоматологической практике мы выбрали 2 заболевания, сопровождающиеся нарушением микроэкологии ротовой полости, - хронические периодонтиты и альвеолиты, развившиеся после удаления зуба. Для лечения альвеолитов мы использовали сухой лиофилизированный порошок Витафлор(r). Применяли следующие схемы - см. схемы 1 и 2. 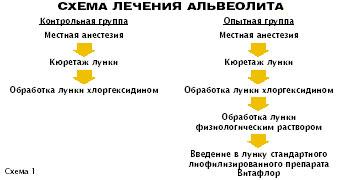 
Это исследование показало эффективность применения пробиотической терапии в лечении дисбиотических состояний: клинический эффект, в случае лечения альвеолитов, выражался в исчезновении болевого синдрома на 1-е сутки и острых воспалительных явлений на 3-и сутки, в то время как у пациентов контрольной группы снижение болевого синдрома проявлялось на 3-и - 5-е сутки, а клиническое излечение - на 7-е - 12-е сутки. Наиболее удобной и эффективной формой препарата при лечении хронических форм периодонтитов является жидкая с вязкостью 0,2% агара, которую удобно использовать при введении в корневой канал, кроме того, в жидкой форме препарата культура бактерий находится в активном состоянии. Данное исследование не является исчерпывающим, но убедительно показывает необходимость применения и включения в комплексную терапию лечения инфекционно-воспалительных заболеваний ЧЛО пробиотических препаратов. Такое лечение позволяет реализовать этиопатогенетический подход в стратегии лечебного процесса. Необходимо помнить, что штаммы пробиотических препаратов обладают собственным спектром и уровнем антагонистической активности и их следует использовать как этиотропный препарат направленного действия.
Также широко известно, что при применении антибиотиков происходит снижение местного иммунитета, неспецифической резистентности и барьерных свойств кожи челюстно-лицевой области, слизистых оболочек органов полости рта (Аразашвили Л.Д. и др., 1999; Дерябин Е.И., 1999); кроме того, сами микроорганизмы, вызывающие патологические процессы, обладают целым рядом иммуносупрессивных свойств (Дальская А.И., Валышев А.В., Елагина Н.Н., Матчин А.А., 1999). Иммуносупрессия приводит к нарушению регенерации раны и к развитию суперинфекции. Для коррекции иммунологических изменений используются иммунотропные препараты, которые подразделяют на иммуномодуляторы, иммунокорректоры, иммуностимуляторы, иммунодепрессанты (Нестерова И.В., Старченко А.А., Иванова С.А., Симбирцев А.С., 2002). Иммунотерапия должна выполняться на фоне обязательного контрольного мониторирования иммунного статуса (Некрасова И.В., 1999). Заподозрить иммунодефицитное состояние можно по характерным клиническим признакам (согласно рекомендациям ВОЗ): несколько подтвержденных отитов или синуситов (не менее 4 - 6 раз в течение года), более 2 подтвержденных пневмоний либо глубоких инфекций (менингит, остеомиелит, сепсис), глубокие абсцессы и флегмоны кожи, персистирующие грибковые заболевания, потребность в терапии антибиотиками. Последнее особенно показательно для иммунодефицита, так как большинство антибиотиков сами не убивают, а лишь блокируют их жизненный цикл. Распознать и уничтожить патоген все равно должна иммунная система. Именно поэтому иммуностимулирующая терапия может дать необходимый толчок для адекватного ответа на патоген. В настоящее время существуют общие принципы применения иммуномодуляторов у больных с недостаточной антиинфекционной защитой:
1. Иммуномодуляторы назначаются в комплексной терапии одновременно с антибиотиками с первого дня их применения.
2. Иммуномодуляторы, действующие на фагоцитарное звено иммунитета, можно назначать больным как с выявленными, так и с невыявленными нарушениями иммунного статуса.
Исследования последних лет показали, что пробиотики способны оказывать иммуномодулирующее действие (Neumann E., Oliveira M.A., Cabral C.M. et al., 1998; Kirjavainen P.V., Nesami H.S., Salminen S.I. et al.,1999; Erickson K.L., Hubbard N.E., 2000; Matsuzaki T., Chin J., 2000; Haller D., Blum S., Bode C., 2000). Весьма интересной и перспективной является способность различных штаммов пробиотиков оказывать разнонаправленное действие на синтез цитокинов, что дает возможность влиять на иммунологические процессы, направляя их по Тh1-типу или по Тh2-типу. Особенно актуальной является способность пробиотиков оказывать противовоспалительное действие (Kato I., Endo-Tanka K., Yokokura T., 1998; Remacken B.J., Snelling A.M., Hawkey P.M. et al., 1999). В настоящее время имеются экспериментальные данные, свидетельствующие об активационном воздействии пробиотиков на фагоцитарную систему и синтез антител как на системном, так и на местном уровнях. Показано, что лактобактерии стимулируют фагоцитарную активность макрофагов (Neumann E., Oliveira M.A., Cabral C.M. et al., 1998), увеличивают количество плазматических клеток (Erickson K.L., Hubbard N.E., 2000), вызывают усиление синтеза IgA и IgM на слизистых оболочках, оказывают регулирующее влияние на уровень IgE (Yasui H., Shida K., Matsuzaki T., Yokokura T., 1999). Установлено, что L.acidophilus увеличивают процентное содержание CD4+-лимфоцитов (Pestka J.J., Ha C.L., Warner R.W. et al., 2001).
Немаловажное значение при коррекции иммунологических состояний в качестве "терапии сопровождения" отводится иммуномодуляторам растительного происхождения - адаптогенам. Данные препараты проявляют выраженные (оптимизирующие иммунитет) свойства: экстракт элеутерококка, препараты эхинацеи (Иммунал и др.), экстракт родиолы розовой (Яременко А.И., 1998) и др. Однако следует внимательно отнестись к назначению адаптогенов (кроме родиолы розовой) и витаминных препаратов (кроме аскорбиновой кислоты). Эти препараты проникают внутрь микробной клетки, увеличивая возможность сопротивления защитным системам организма и тем самым усиливая патогенность.
Примером "терапии сопровождения" может являться приведенная ниже схема:
1. Нутриционная поддержка;
2. Прием витаминных препаратов и микроэлементов (аскорбиновая кислота по 500 - 1000 мг 2 раза в день);
3. Прием энтеросорбентов (полифепан по 1 столовой ложке 3 раза в день);
4. Прием иммунотропных препаратов и адаптогенов (экстракт родиолы розовой по 20 капель 2 раза в день);
5. Прием пробиотических препаратов (Витафлор(r) 1 флакон лиофильновысушенной культуры растворить в 100 мл воды, производить ирригации полости рта с последующим проглатыванием раствора, применять 3 - 4 раза в день по 2 столовые ложки в течение курса антибактериальной терапии).
Таким образом, включение в комплекс лечебных мероприятий инфекционно-воспалительных заболеваний челюстно-лицевой области некоторых элементов "терапии сопровождения" целесообразно для уменьшения вероятности развития местных и системных осложнений как от основного заболевания, так и от медикаментозной терапии. Использование биопрепаратов с доказанной эффективностью приводит к улучшению результатов лечения.

|



