
А.И. Яременко, к.м.н., доцент кафедры хирургической стоматологии и челюстно-лицевой хирургии СПбГМУ им. акад. И.П. Павлова
С.Ю. Виноградов, врач, клинический ординатор кафедры хирургической стоматологии и челюстно-лицевой хирургии СПбГМУ им. акад. И.П. Павлова
.
Фармакологическая поддержка больных при имплантологическом лечении
  Развитие имплантологии, равно как и возросшие требования, предъявляемые пациентами, неминуемо ведут к изменению подходов к лечению и созданию оптимальных схем фармакологической поддержки при проведении имплантологического лечения.
Основными звеньями успешной фармакотерапии при проведении лечения являются:
1. Профилактика ранних воспалительных осложнений;
2. Профилактика нарушений
в микроциркуляторном русле;
3. Оптимизация остеоинтеграции имплантата;
4. Оптимизация заживления мягких тканей.
Одной из остро стоящих задач является профилактика инфекционно-воспалительных процессов в послеоперационной ране, развитие которых ставит под угрозу результат операции.
Известно, что предотвращение осложнений значительно проще и безопаснее, чем борьба с развившимся процессом. Традиционно для этих целей используются антибактериальные препараты и антисептики, но не стоит забывать и о мануальных методах профилактики: сокращение времени операции за счет использования современных методик, борьба с госпитальной инфекцией, строгое соблюдение принципов асептики, обученность кадров и хорошее техническое оснащение операционной. Необходимо учитывать биофизические аспекты препарирования ложа под имплантат (использование острых фрез с оптимальной геометрией инструмента для отвода стружки, адекватное охлаждение, соблюдение рекомендуемого скоростного режима, прерывистое препарирование).
Известно, что около 30% назначений антибиотиков осуществляется с профилактической целью. В хирургической практике различают предоперационную, интраоперационную и послеоперационную антибиотикопрофилактику осложнений. Наибольшее распространение получила предоперационная антибиотикопрофилактика. Для адекватной химиопрофилактики необходимо создание в биологических жидкостях достаточной концентрации противомикробного вещества. Известно, что правильно спланированная антибиотикопрофилактика снижает удельный вес осложнений с 40% до 5%.
Одним из основных факторов, влияющих на вероятность развития раневой инфекции, является степень микробной обсемененности. В зависимости от нее операции подразделяются на 4 группы (Keighley M., 1982; Keinbaum S., 1983; Classen D.C., 1992):
- "чистые" операции (риск менее 5%) - операции, проводимые без дополнительных разрезов мягких тканей ("flap free surgery");
- "условно-чистые" (риск около 10%) - малотравматичные операции, связанные с длительной экспозицией раны, широкой отслойкой лоскутов;
- "загрязненные" (риск около 20%) - иплантация непосредственно после удаления зубов, все виды аугментации;
- "грязные" (риск около 30 - 40%) - операции в заведомо инфицированных областях, установка имплантатов непосредственно после удаления зуба по поводу хронического инфекционно- воспалительного процесса, подъем дна верхнечелюстного синуса при хроническом воспалительном процессе в пазухе, аугментация с использованием внеротовых донорских участков и т. д.
Для профилактики осложнений необходимо соблюдать и организационные мероприятия (сокращение времени операции за счет использования современных методик, борьба с госпитальной инфекцией, строгое соблюдение принципов асептики, обученность кадров и хорошее техническое оснащение операционной).
При планировании антибиотикопрофилактики необходимо учесть следующие правила проведения антибиотикопрофилактики:
- введение антибиотиков должно начинаться не раньше, чем за 1 час до операции, и не позже, чем за 30 мин. Применение препарата менее чем за 30 мин. не снижает риска развития осложнений;
- выбранный антибиотик должен быть активен в отношении эндогенной микрофлоры больного (периоперационные посевы), в отношении госпитальной микрофлоры (эпидемиологическая обстановка);
- период полувыведения антибиотика должен совпадать или превышать длительность операции;
- если рана широко сообщается с полостью рта и при этом существуют дополнительные факторы, способные вызвать инфекционно-воспалительный процесс, то назначение антибактериальной терапии показано и в послеоперационном периоде (5 - 7 дней);
- препарат должен обладать минимальными побочными эффектами.
Необходимо отметить, что цефалоспорины 1-го и 2-го поколений считаются основной группой препаратов для антибиотикопрофилактики, но по ряду показаний должны назначаться в комбинации с другими антибиотиками.
Наиболее перспективным для антибиотикопрофилактики на сегодняшний момент представляется b-лактамная группа. Хорошее проникновение в ткани и удовлетворительная переносимость позволяет использовать эту группу для пред-, интра- и послеоперационной профилактики. Наиболее эффективной является монотерапия амоксициллином/клавуланатом (аугментин, амоксиклав). Комбинация амоксициллина и ингибитора b-лактамаз (клавулановой кислоты) дает препарату большие возможности по спектру действия. Клавулановая кислота не обладает сколько-нибудь значимыми антибиотическими свойствами, однако имеет сродство к ферментам b-лактамазам, являясь их необратимым ингибитором, что предотвращает разрушение амоксициллина. Кроме того, она добавляет амоксициллину активность в отношении практически всех антианаэробных возбудителей. Амоксиклав внутрь применяется по 625 мг 3 раза в сутки или по 1000 мг 2 раза в день. При парентеральном введении препарата дозировка составляет 1 - 2 г 3 раза в день внутривенно.
Перед операцией, не ранее чем за 1 час, производится прием препарата внутрь или внутривенное введение, дальнейшее введение производится с учетом фармакодинамики препарата не менее 5 суток после операции.
При профилактическом применении антибиотиков в 4-й группе наиболее целесообразным является предоперационное введение, послеоперационное введение препарата.
При использовании амоксиклава прежде всего достоверно снижается вероятность диссеминации операционной раны патогенными и условно-патогенными микроорганизмами и обеспечивается антимикробная активность в ране на протяжении 8 часов.
При длительных операциях также можно использовать антибиотики с длительным периодом полувыведения (цефтриаксон 1 - 2 г. За 30 - 90 мин. до операции, цефотаксим - 1 - 2 г во время вводного наркоза, цефуроксим 1,5 г, метронидазол 500 мг - 1 г перед введением в наркоз).
В последнее время получила распространение сочетанная антибиотикопрофилактика, которая заключается в системном применении антибиотика и местном использовании антисептика. В качестве антисептика наиболее часто используют препараты на основе хлоргекседина биглюконата 0,05 - 0,2%. Согласно исследованиям, данные антисептики являются цитотоксичными и нарушают клеточную дифференцировку и пролиферацию, что, безусловно, не оптимизирует процесс регенерации. Длительная экспозиция раны приводит к открытию сайтов адгезии для патогенных и условно-патогенных микроорганизмов на ее поверхности, кроме того, подавление резидентной (стабилизирующей) флоры при использовании антисептиков с точки зрения микробной экологии приводит к дисбиотическому сдвигу в микробиоценозах слизистой полости рта (рис. 1).
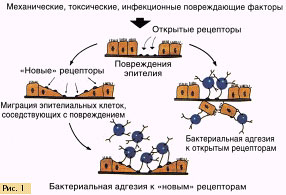
Мы полагаем, что этио-патогенетически обосновано применение бактерийных препаратов. В клинической практике для коррекции нарушений внутренней микробной экологии используются различные препараты:
1. Пробиотики - это препараты, содержащие живые, активные микроорганизмы и их метаболиты, которые сохраняют или восстанавливают состав нормальной микрофлоры. Пробиотики могут содержать как монокультуру - один штамм микроорганизма (Лактобактерин, Бифидумбактерин, Бифилин, Ацилакт, Нормофлорин и др.), так и представлять механическую композицию разных видов микроорганизмов (Линекс, Бификол, Бифилонг и др.). Комбинированные препараты, содержащие виды микроорганизмов, образующих симбиоз, именуются симбиотиками (Витафлор). Препараты последней группы более эффективны, так как симбиоз бактерий усиливает их полезные свойства.
2. Пребиотики - препараты, не содержащие живых микроорганизмов и селективно стимулирующие рост и активность симбионтной микрофлоры (Лактулоза, Хилак-Форте и др.).
3. Синбиотики - комплексные препараты про- и пребиотиков (Бифиформ, Ламинолакт и др.).
По нашему мнению, применение пробиотических препаратов обосновано, так как содержащиеся в их составе жизнеспособные микроорганизмы, помимо восстановительной функции микробиоценозов, сами обладают антагонизмом по отношению к патогенной и условно-патогенной микрофлоре и участвуют в регуляции каскада иммунологических реакций (Б.А. Шендеров, 1998; Л.Н. Петров, 2002).
Механизм лекарственного действия пробиотических препаратов можно представить, опираясь на данные по ауторегуляции в бактериальных популяциях. При попадании в организм штамм пробиотического микроорганизма выделяет в окружающую среду низко- и высокомолекулярные метаболиты. Низкомолекулярные метаболиты влияют на состав микробиоцинозов, восстанавливая его, в то время как высокомолекулярные метаболиты ответственны за проявления антагонистической активности по отношению к патогенным и условно-патогенным микроорганизмам. Кроме того, метаболиты разной химической природы и различного молекулярного веса обладают иммуномодулирующим действием (Nicole M de Roos and Martijin B Katan, 2000). Поэтому нельзя не согласиться с предложением академика А.В. Воробьева называть пробиотики - иммунобиотиками.
Вместе с тем, как показывает клиническая практика, эффективность пробиотической терапии зависит от грамотного применения препарата определенного типа, лекарственной формы, способа и схем его применения.
На наш взгляд, одним из перспективных препаратов для коррекции микроэкологических нарушений и восстановления иммунологической резистентности является пробиотик нового поколения, симбиотического действия - Витафлор(r), разработанный в ГосНИИ особо чистых биопрепаратов, Санкт-Петербург. Наш выбор препарата основывался на доказанной безвредности применения препарата, высокой метаболитической активности штаммовой культуры, уровне и спектре антагонизма и устойчивости к антибиотикам, выраженных адгезивных свойствах препарата, что определяет длительность действия. Отличительной особенностью препарата является наличие симбиотической биокультуры Lactobacillus аcidophilus (штаммы Д № 75 и Д № 76) (рис. 2).
 В отличие от моноштаммов, биокультура препарата характеризуется расширенным спектром и высоким уровнем антагонистической активности в отношении Гр(-) и Гр(+) бактерий и дрожжевых грибов рода Candida, выраженными адгезивными свойствами, высоким содержанием жизнеспособных клеток (не менее 5(108 КОЕ в одной дозе) (рис. 3). Штаммы биокультуры образуют симбиоз, что повышает жизнеспособность бактериальной основы, которая непосредственно коррелирует с терапевтической активностью препарата.
 Мы использовали сублингвальную форму препарата Витафлор(r) (по 1 таблетке 3 раза в день в течение 7 - 14 дней), а также жидкую форму (1 флакон лиофильно-высушенной культуры растворяли в 100 мл воды и производили полоскания полости рта с последующим проглатыванием раствора 3 - 4 раза в день по 2 столовые ложки).
Любое медикаментозное вмешательство, а тем более хирургическая операция - это не только боль, но и в определенной степени агрессия, которой подвергается организм пациента, вызывающая целый комплекс компенсаторно-приспособительных реакций. Во время вмешательства больной переживает так называемый операционный стресс. Стресс-норма на хирургическую агрессию не определена. Ведущим механизмом стрессорных реакций является стимуляция через гипоталамус и другие центры среднего мозга вегетативной нервной системы с последующим выбросом в ток крови адреналина. Длительно существующее, высокое по интенсивности стрессирующее воздействие (например, боль или интраоперационный стресс) способно вызывать реакцию дистресса (Г. Селье, 1974). Перераздражение адреналиновой системы сменяется резким повышением активности парасимпатической нервной системы, приводящим к развитию ишемии и тканевой гипоксии в области раны, что отрицательно влияет на процессы регенерации. Таким образом, устранение боли в пред- и послеоперационном периоде является сугубо патогенетической мерой. Отчасти предоперационное устранение боли решается с помощью современных амидных анестетиков и трехступенчатой методикой проведения анестезии: на первом этапе проводится аппликация местноанестезирующего средства на 1 - 15 мин. в области вкола, далее проводится подслизистое введение 0,2 - 0,3 мл анестетика, через 2 мин. окончательное создание депо анестетика. Наиболее оправданным как в предоперационном является применение комплекса мероприятий, направленных на предупреждение интра- и послеоперационных осложнений, то есть премедикации.
Виды премедикации:
1. Психоэмоциональная (беседа с пациентом и выявление тревожности);
2. Физическая (физиотерапевтические методы, например, гальванический воротник по Щербаку);
3. Медикаментозная (использование различных групп фармакологических средств).
Существует огромное количество схем для премедикации. Их выбор основан на особенностях каждого больного и объема вмешательства. Седативная премедикация
Заключается в уменьшении или подавлении физиологических и психологических реакций на стресс без потери сознания.
Группы:
(1) бензодиазепины (диазепам 0,005 - 0,01 г, феназепам 0,0005 - 0,001 г; элениум 0,01 г; дормикум 0,5 - 0,75 мг/кг - начало действия через 10 мин., длительность 1,5 - 2 часа, затем наступает ретроградная амнезия);
(2) седативно-снотворные (настойка валерианы 60 кап., пустырника 60 кап., корвалол 30 кап.);
(3) антигистаминные (димедрол 0,5 - 1,0 мг/кг).
Анальгетическая премедикация
Наиболее оправданным как в предоперационном, а тем более в послеоперационном периоде является использование нестероидных противовоспалительных препаратов, которые кроме анальгезирующего действия обладают гипосенсебилизирующим, антипиретическим, антиагрегационным эффектами.
Ксефокам (лорноксикам) - нестероидный противовоспалительный препарат класса оксикамов с выраженным анальгетическим действием. В основе механизма действия лорноксикама лежит угнетение синтеза простагландинов вследствие сбалансированного угнетения активности изоферментов циклооксигеназы-1 и циклооксигеназы-2. Применять препарат следует за 30 мин. до операции 8 мг внутримышечно, в послеоперационном периоде по 8 мг по 1 таблетке 2 раза в день.
Залдиар - комбинированный препарат, содержащий трамадол и парацетамол. Трамадол - синтетический опиоидный анальгетик центрального действия, обеспечивающий мощный и продолжительный обезболивающий эффект. Парацетамол - один из наиболее безопасных анальгетиков-антипиретиков. Парацетамол и трамадол в используемой комбинации обладают синергизмом в отношении обезболивающего действия. Благодаря парацетамолу наступает быстрое обезболивание, в то время как трамадол обеспечивает пролонгированный эффект. Обезболивающий эффект при приеме Залдиара наступает менее чем через 20 мин. и сохраняется более 5 часов. Начальная рекомендуемая доза - 1 - 2 таблетки. Интервал между приемами должен быть не менее 6 часов. Максимальная суточная доза - 8 таблеток (300 мг трамадола и 2,6 г парацетамола).
Подавление рвотного рефлекса
Пипольфен по 25 мг или дедалон (димедрол + хлортеофиллин) по 50 мг за 30 мин.
Примером схемы премедикации может явиться схема по Задорожному:
1. Кетанов (0,01 г - 1 - 2 таб.);
2. Димедрол (0,05 г - 1 таб.);
3. Метацин (0,004 г - 2 таб.).
В основе интеграции имплантата с костной тканью лежат не только генетически запрограммированные механизмы регенерации кости, но и целый ряд физико-химических реакций. Немаловажным является управление механизмами костной интеграции путем создания условий, обеспечивающих запуск механизмов регенерации кости, а также создание соединительно-тканного барьера на уровне слизистой оболочки.
К препаратам, оптимизирующим процессы метаболизма в костной ткани, относятся стимуляторы остеогенеза и препараты, способствующие адекватной минерализации костного матрикса.
К стимуляторам остеогенеза относятся такие препараты, как Остеогенон, который оказывает двойное действие на метаболизм костной ткани при остеопорозе: анаболическое, за счет активации остеобластов, и антикатаболическое, за счет торможения функции остеокластов. Остеогенон содержит необходимые компоненты для синтеза костной ткани: органический компонент содержит ряд белков, синтезирующихся в норме клетками костной ткани (трансформирующий фактор роста бета (TGF-beta), инсулиноподобные факторы роста I и II (IGF-I, IGF-II), остеокальцин, коллаген первого типа) и оказывающих регулирующее действие на процессы костеобразования и резорбции кости. Препарат применяют по 2 таблетки 2 - 3 раза в сутки. Остеохин (Иприфлавон) - синтетическое производное природных флавоноидов; улучшает метаболизм костной ткани, снижает ее резорбцию. Применяют внутрь, после еды, по 200 мг 3 раза в день. Курс лечения - от 6 месяцев до 3 лет. Назначение данных препаратов наиболее оправдано при III, IV типах архитектоники костной ткани.
Группу препаратов, способствующих адекватной минерализации костного матрикса, составляют соединения кальция в комплексе с витаминами и микроэлементами.
Остео Плюс - витаминно-минеральный комплекс, применяют по 2 таблетки 2 раза в день во время еды.
Кальций Магний Хелат - комбинированный препарат, содержащий витамин D (рыбий жир) - 133 МЕ; кальций (хелат, цитрат) - 250 мг; магний (хелат, оксид) - 100 мг; фосфор (хелат) - 100 мг. Применяют по 2 таблетки 2 раза в день во время еды.
Остеокальцин и другие препараты.
Не стоит забывать, что биохимические процессы в костной ткани сбалансированы и контролируются и регулируются эндокринной системой. Регулирующее влияние на деятельность остеобластов и остеокластов оказывают половые гормоны (эстрогены и андрогены). Известно, что эстрогены оказывают действие на предшественников остеобластов, а также ускоряют пролиферацию и дифференцировку остеобластов, кроме того, эстрогеновые рецепторы обнаружены на остеокластах и, взаимодействуя с ними, замедляют активность этих клеток, а следовательно, и костную резорбцию. Одним из путей оптимизации остеогенеза является использование низкодозовой гормонотерапии эстрогенами (можно использовать трансдермальный пластырь "Климара"). Для стимуляции анаболических процессов допустимо введение анаболических стероидов после консультации с эндокринологом.
Немаловажным аспектом при имплантации является соединительно-тканная интеграция имплантата на уровне слизистой оболочки десны, которая тесно связана с процессом остеогенеза в области альвеолярного отростка. Для оптимизации соединительно-тканной интеграции необходимо использовать кератопластические средства: солкосерил адгезивная денальная паста и др., кроме того, пародонтальные повязки, такие, как Septopack, которые не обладают свойствами, оптимизирующими регенерацию, но защищают операционную рану и линию швов от неблагоприятных факторов полости рта (микроорганизмов, термических и механических факторов и т. д.), способствуя этому процессу опосредованно.
Таким образом, рациональное использование фармакотерапевтических средств позволяет избежать осложнений на этапах имплантации и сделать лечение для пациента комфортным, а для врача прогнозируемым.

|



